

a aerului cu continut de hidrocarburi
Carbonul are simbolul
C, element crucial al existentei organismelor sicare are mai
multe aplicati industriale. Numarul atomic al C este 6; elementul
este in gr. a IV al sistemului periodic al elementelor.
Proprietati: Greutatea atomica a C este 12,01115. Cele 3 stari
naturale ale carbonului sunt- diamantul, granitul si carbonul
amortiu -ele sunt solide cu o temperatura de topire extrem de
ridicata sisunt insolubile in toti solventii la temperaturi
normale. Proprietatile fizice ale celor 3 tipuri de C nu prea
difera din cauza diferentelor in structura cristalina. În
diamant, cel mai dur material cunoscut, fiecare atom este in
legatura cu alti 4 atomi intr-un schelet 3D, granitul consista in
legaturi saptamânale de straturi de atomi care sunt aranjati in
hexagon. C amorfiu este caracterizat de un grad scazut de
cristalinitate. C amorfiu pur poate fi obtinut prin incalzirea
zaharului la 900 grade in absenta aerului. C are abilitatea unica
de a face legaturi cu alti atomi de C pentru a forma, lanturi si
inele complexe. Aceasta proprietate duce la un numar aproape
infinit de compusi ai carbonului cel mai comun element fiind cel
care contine C si H2.Primii compusi ai C au fost identificati in
materia vie la inceputul sec 19. La temperaturi normale C are o
radioactivitate scazuta. La Temperaturi ridicate reactioneaza cu
aproape toate metalele pentru a forma carburi, iar cu oxigenul
formeaza monoxidul de carbon si dioxidul de carbon. De asemenea
carbonul formeaza compusi cu multe elemente nemetalice desi unele
ca si C tetraclorid trebuie format indirect.
Se gaseste: C nu este un element raspandit in natura desi este
intr-un procent de 0,025% din atmosfera Pamantului. Se gaseste
cel mai des sub forma de carbonat. Co2 este un compus important
al atmosferei si este principala sursa de carbon incorporat in
materia vie . Plantele folosind fotosinteza transforma Co2 in
compusi organici de carbon care este consumat de alte organisme.
C amorfiu se gaseste in grade variabile de puritate in carbuni ,
cox.
In 1985 oameni de stiinta au evaporat granit pentru a forma o
molecula de carbon stabil format din 60 de molecule de C avand
forma unei sfere. Molecula a fost numita buckminsterfullerene.
Aplicatii stintifice: Cle mai comun izotop al C este carbon-12 ;
in 1961 acest izotop a fost ales pentru a inlocui izotopul
oxigenului16 ca standard al greutatii atomice, si a fost data
greutatea atomica 12.
Izotopul C-13 si 4 sunt folosite extensiv ca urme in cercetarile
biochimice. C14 este asemenea folosit in tehnica numita datarea
cu carbon radioactiv care permite gasirea varstei fosilelor si
altor materi organice. C 14 este produs in continuu in atmosfera
de razele cosmice si se afla in orice materie vie.Cum carbonul 14
se descompune cu jumatate de viata de 5760 de ani.
l |
 |
 |
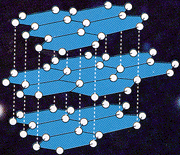
| Diamant | Grafit | Fulerena(Articol-Click pe imagine) |
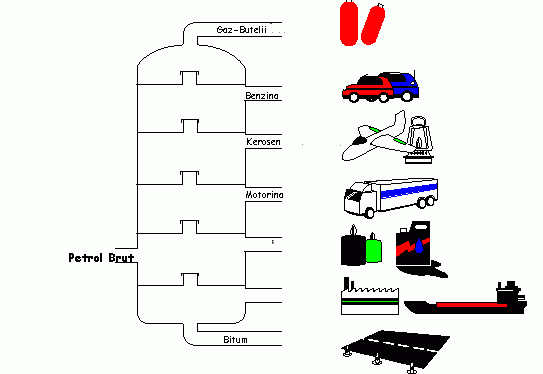
In limba latina,
echivalentul pentru petrol- ''Petrolum'' semnifica ulei de
piatra; nafta (In greaca- ''naphtha''); titei- substanta minerala
lichida lichida sau vascoasa, combustibila, constituita dintr-un
amestec de hidrocarburi solide, lichide sau gazoase din clasa
metonica (parafinica), naftenica si aromatica cu un mic adaos de
alti compusi organici:
· de sulf (0,1 - 6%)
· de oxigen (pana la 5 %), azot s.a.
In medie petrolul contine 85% C, 12-14% H, restul revine N, O, S,
V, Co, Cu, P, K, I, Fe s.a. Petrolul este uleios, florescent, de
culoare bruna Inchisa sau neagra cu nuante verzui sau galben
verzui. Exista si petrol galben- deschis, straveziu, petrol
''alb'' ce se gaseste In Baku si Pensylvania. Petrolul cu apa
formeaza emulsii stabile. Dupa densitate se deosebesc:
· Petr. usoare (densitatea 730-900 kg/m*3*);
· Petr. grele (densitatea 900-1040 kg/m *3*).
Puterea calorica a petrolului este Intre 10000 si 11000 cal./kg.
In functie de hidrocarburile predominante (peste 50%) se
deosebesc:
· Petrol metanic (parafinic);
· Petrol naftenic (cicloparafinic);
· Petrol aromatic.
Exista si petrol mixt, de exemplu petrol nafteno- metanic (25%
hidrocarburi naftenice si peste 50% metanice).
In natura petrolul se acumuleaza In roci poroase strabatute de
pisuri, numite roci- colectoare sau roci- magazii. Acestea pot fi
gresii, nisipuri, calcare, dolomite, s.a. De obicei In rocile-
magazii petrolull se gaseste In asociatie cu cu gazele naturale.
Geneza petrolului nu este definitiv stabilita. Exista doua
teorii: organica si anorganica.
Pe fundul marilor se amesteca si putrezesc organizme animale si
ramasite vegetale, In a caror structura intra carbonul si
hidrogenul: diatomee, protozoare, radiolari, alge unicelulare,
saprofite, plancton etc.Ferite de contactul cu aerul, sub
straturi de sedimente nisipoase, materiile organice se
acumuleaza, se Incing si se descompun. Datorita microbilor
anaerobi, ele fermenteaza si se transforma Incet, dand nastere
unor mase vascose sau gazoase de hidrocarburi, pe care le numim
cu un singur cuvant- petrol. Atat petrolul cat si gazele de
sonda, care se formeaza In pungile ascunse sau deasupra vechilor
depozite marine, au rezultat printr-un proces de bituminizare a
materiei organice, care a format depozite numite sapropel
(amestec de hidrocarburi solide, lichide, gazoase) sub actiunea
unor bacterii ca Bacterium aliphaticum si Methanomas methanica.
Hidrocarburile solide sau vascose (bitumen, asfalt) s-au format
din petrol, care si-a pierdut hidrocarburile gazoase. Lor li se
adauga sisturile bituminoase, care sunt argile sau marne bogate,
Imbinate de materie organica. Acestea din urma reprezinta o
importanta rezerva strategica de energie a industriei. Prin
urmare, conform primei teorii, petrolul se formeaza din substanta
organica dispersata In rocile sedimentare depuse pe fundul
bazinelor acvatice (mari, oceane, lacuri, lagune) In conditii
anaerobe. Astfel de roci se numesc roci- mama. La cufundarea
rocilor- mama In interiorul scoartei terestre la adancimi de
peste 1 km, In urma actiunii proceselor tectonice se creeaza
anumite conditii termodinamice, datorita carora, din substantele
organice incluse In aceste roci se degaja hidrocarburile lichide
si componenti gazosi (CO*2* si NH*4*). In urma compactizarii
rocilor- mama, hidrocarburile si componentii gazosi migreaza In
stratele de roci poroase (rezervoare naturale), acumulandu-se In
asa- numitele ''captoare''.
Una din teoriile anorganice presupun formarea petrolului din
capiturile magnatice din adancul pamantului, de unde acestea
patrund In scoarta terestra si la suprafata ei prin rupturile
tectonice de adancime.
Petrolul constitue sursa principala de combustibili lichizi,
precum si de materie prima pentru industria chimica, servind la
prelucrarea celor mai diverse produse (cauciuc, solventi,
explozibili, detergenti etc).
Cercetarile de specialitate au stabilit ca petrolul- supranumit
In mod justificat si ''aurul negru'', pentru calitatile si
avantajele pe care le ofera- s-a impus printr-o continua si
remarcabila diversificare a utilizarii lui In cursul istoriei,
fiind prezent ''pretutindeni, universal si multiplu dintotdeauna,
etern si misterios''. In ultimul secol acesta a devenit un produs
extrem de cautat, absolut necesar desfasurarii vietii economice
moderne, un factor important al politicii internationale si
indispensabil In vreme de razboi, provocand dese si aprinse
conflicte diplomatice si economice, batalii ''reci'' sau
''calde'', tensiuni si suspiciuni Intre state si natiuni. La
sfarsitul sec. al XIX- lea, Inceputul sec. al XX- lea s-a trecut
pentru prima data la utilizarea derivatelor obtinute din
extragerea ''aurului negru'' drept combustibil. In a doua
jumatate a veacului trecut, singur lampanul- produs obtinut din
distilarea petrolului sau titeiului- era solicitat cel mai adesea
pe piata, el servind prin excelenta la iluminat. Celelalte
subproduse petroliere mult folosite si cerute astazi (pacura sau
mazutul, esenta sau benzina, uleiurile minerale, parafina s.a)
erau prea putin cunoscute ori nu-si gasisera o Intrebuintare
larga. Interesul pentru petrol a crescut brusc o data cu
inventarea motorului cu combustie interna In ultimul deceniu al
secolului trecut. Dupa cum se stie, In anul 1897, Diesel a
brevetat motorul, ce-i poarta numele, functionand exclusiv pe
baza de pacura si care a capatat curand o larga utilizare In
industrie, cai ferate, marina comerciala si militara etc.
Carbunele, combustibil solid care In a doua jumatate a secolului
al XX- lea a contribuit substantial la prosperarea economica a
Marii Britanii, Germaniei si a S.U.A., a Inceput sa fie concurat
serios de catre combustibilul lichid- adica de petrol- a fost de-
a dreptul spectaculoasa. Astfel este de ajuns sa amintim ca deja
In anul 1930 peste 26% din energia mondiala era furnizata de
petrol, In vreme ce astazi proportia respectiva s-a dublat.
Aceasta ascensiune rapida s-a datorat indiscutabil avantajelor
multiple pe care le-a prezentat din primul moment petrolul, fata
de carbune, ca producator de energie:
· randamentul superior (1 kg titei = 1,7 kg carbune);
· extractia mai usoara;
· lesne de transportat (prin pipe-lines-uri) si In scurt timp,
cu minim de pierderi;
· transport pe mare In conditii mai avantajoase (Incarcare,
securitate, volum etc.);
· prin calitatile lor, produseler petroliere asigura vaselor
comerciale sau de razboi o raza de actiune superioara si o mare
mobilitate.
Larga utilizare pe care a capatat-o petrolul a avut drept
rezultat cresterea rapida a cererii mondiale de combustibil
lichid. Acest lucru a determinat, la randul sau, sporirea In
adevarate salturi a productiei de titei, care a devenit un produs
extrem deapreciat si de cautat, mai ales datorita repartitiei lui
inegale pe glob. Astfel, In timp ce Intre 1857 si 1900 productia
mondiala anuala de titei a urcat de la 275 tone la 22,3 milioane
tone, ea atinsese deja 104,9 milioane tone, pentru ca In anul
1927 sa se cifreze la 172,8 milioane tone. Sporul Inregistrat
fata de 1900 reprezenta, asadar, 500% In 1921 si circa 1000% In
1927.
Combustibilul lichid a fost produsul care a favorizat (prin
reunirea unor mari capitaluri necesare cercetarii si extragerii
lui, prin constituirea unor puternice Intreprinderi, dezvoltate
vertical si orizontal, pentru prelucrarea, desfacerea si
transportul lui etc.) Inchegarea unor puternice organizatii
capitaliste. Astfel, primul trust capitalist - Standard Oil Co.-
a fost fondat tocmai In domeniul industriei petroliere de John
Rockefeller In 1882.
In decursul catorva decenii petrolul s-a transformat Intr-unul
din elementele fundamentale ale vietii economice moderne. El a
devenit- dupa expresia fericita a lui Anton Zischka- ''sangele
economiei''. Forarea primului put de catre ''colonelul'' nord-
american Edwin L. Drake a avut loc In 1859. Deci, petrolul nu
numai ca a fost factorul decisiv In prosperarea industriei,
oferind numeroase facilitati si avantaje, ci a si reprezentat un
element important In viata internationala.
Benzenul este cel mai
simplu si totodata cel mai important reprezentant al
hidrocarburilor aromatice, o grupa de substante care se deosebesc
in multe privinte de cele studiate pana acum. Proprietatile
hidrocarburilor aromatice precum si influentele pe care le
exercita resturile acestor hidrocarburi asupra celorlalte grupari
din moleculele in care sunt prezente, au un caracter specific.
Acesta consta in mare parte dintr-o imbinare a unor insusiri
proprii substantelor nesaturate, cu insusiri racteristice
compusilor saturati. Din aceasta imbinare rezulta si o serie de
proprietati cu totul noi. Toate acestea fac sa existe si astazi
tratate in care chimia organica este impartita in studiul a doua
serii: seria alifatica cuprinzand alcanii, alchenele, acetilenele
si derivatii acestora, si seria aromatica, in care se includ
hidrocarburile aromatice si substantele care deriva de la
acestea.
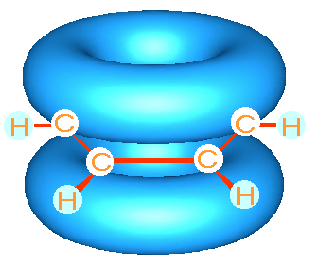
Molecula benzenului este alcatuita din 6 atomi de carbon si 6
atomi de hidrogen, dupa cum reiese din formula sa moleculara.
Toate datele de care dispune stiinta dovedesc echivalenta
perfecta a celor 6 atomi de carbon precum si a celor 6 atomi de
hidrogen, avand astfel o structura ciclica, de asemenea intreaga
structura este plana. Intrucat stabilitatea moleculei de benzen
exclude posibilitatea ca acesta sa reprezinte un compus de tipul
radicalilor liberi, cu 6 electroni desperecheati, solutia cea mai
naturala a problemei ar parea sa fie dupa regulile folosite de
noi pana acum, utilizarea celor 6 electroni pentru a forma 3
perechi de electroni. Aceasta solutie a fost propusa acum 100 de
ani de catre August Kekule, caruia I se datoreaza de altfel si
atribuirea unei structuri ciclice pentru molecula de benzen.
Formula lui Kekule foarte larg utilizata si astazi datorita
faptului ca reda corect multe din caracteristicile moleculei de
benzen, presupune existenta a 3 duble legaturisi a 3 simple
legaturi asezate simetric in molecula benzenului. Toti atomii de
carbon sunt identici intre ei, iar conjugarea are loc intr-un
sistem ciclic inchis. In consecinta, nimic nu stanjeneste
egalizarea deplina a legaturilor simple si duble din molecula
benzenului deci C–C este echivalent cu C=C. Astfel in cazul
benzenului se ajunge la un sistem de electroni ð extins asupra
integii molecule, trasatura fundamentala a structurii
combinatilor numite aromatice si careia i se datoreaza toate
proprietatile cu adevarat specifice acestei clase de compusi
organici.
Doi atomi de carbon vecini se gasesc la o departare de 1,39?,
fata de 1,54? cat masoara legatura simpla si 1,33? cat are
legatura dubla. Calculele arata ca o lungime de 1,39? corespunde
unei legaturi exact "jumatate simpla – jumatate
dubla". Intregul ansamblu de 6 atomi de carbon si 6 atomi de
hidrogen asezati in colturile unui hexagon regulat, toti in
acelasi plan, formeaza ceea ce se numeste nucleu benzenic.
Starea de echilibru stabil, saraca in energie, datorita
aromaticitatii, face ca molecula benzenului desi contine elctroni
ð, sa nu aiba reactivitatea caracteristica alchenelor. Neavand
duble legaturi localizate, iar sistemul conjugat neavand capete,
benzenul nu va avea tendinta de a da nici adtitii 1,2 (la duble
legaturi ca alchenele) nici adtii 1,4, 1,6, etc. (ca butadiena).
Desigur pentru chimia organica moderna aproape nimic nu este
imposibil si s-au gasit mijloace de a forta molecula de benzen sa
dea unele reactii de aditie dar aceasta se realizeaza impotriva
tendintelor naturale ale moleculei.
In locul reactiilor de aditie, reactiile caracteristice pentru
comportarea chimica a benzenului si a hidrocarburilor aromatice
in general sunt reactiile de substitutie. Din acest punct de
vedere, benzenul este mai apropiat de compusii saturati decat de
alchene. Existenta electronilor ð in molecula isi spune insa si
aici cuvantul astfel ca legaturile C – H se rup mai usor
decat la compusii saturati, iar aceasta rupere are loc mai ales
in conditii heterolitice.
Caracterul aromatic reprezinta o consecinta a existentei unui
sistem de electroni ð delocalizati, care interactioneaza intre
ei intr-o zona extinsa asupra intregii molecule, si nu limitata
la spatiul dintre doi atomi legati printr-o covalenta multipla.
Sistemul de electroni ð aromatic cere o molecula plana si cu
structura ciclica. Denumirea de substante aromatice are numai un
caracter istoric si poate sa nu aiba nimic in comun cu mirosul
acestor substante.
La benzen prin unirea zonelor ocupate de electronii ð se
formeaza doua inele asezate de o parte si de alta a planului
hexagonului regulat format de legaturile ó. Prin aceste inele
electronii se pot misca in cerc dar deoarece electroni in miscare
inseamna curent electric rezulta ca in molecula de benzen (si a
altor compusi aromatici) se formeaza adevarate bobine de
inductie, curentii circulari producand ca in orice bobina campuri
magnetice. Aceste campuri magnetice vor influenta puternic
orientarea micilor magneti pe care ii formeaza, dupa cum stim,
nucleele de hidrogen (protonii). Astfel in spectrele de rezonanta
magnetica nucleara care studiaza tocmai deosebirile de stare
magnetica a diferitilor protoni din molecula, atomii de hidrogen
legati direct de nuclee aromatice, dau semnale situate in cu
totul alte regiuni ale spectrului decat cei din gruparile metil,
etil, etc.
Benzenul exista in cantitati reduse in stare naturala in unele
petroluri. In general acestea nu constituie o sursa rentabila
pentru obtinerea benzenului. Exista numeroase cai de sinteza a
benzenului, fie plecand de la produsi de substitutie a ai
acestuia si indepartand substituentii (respectiv inlocuindu-i cu
atomi de hidrogen), fie realizand chiar inchiderea ciclului.
Prima varianta nu are decat importanta stintifica fiind utilizata
mai ales in trecut, cand nu existau metode moderne de analiza,
drept dovada a prezentei nucleului benzenic intr-o anumita
molecula. In schimb cea de-a doua varianta, inchiderea ciclului,
are insemnatate practica pentru prepararea benzenului.
Benzenul este un lichid incolor, foarte mobil, avand un miros
puternic si caracteristic. Benzenul se solidifica la +6°C, ceea
ce produce unele limitari in utilizarea lui ca solvent si cere ca
recipientele in care este pastrat sa fie prevazute cu instalatii
de dezghetare in timpul iernii. Punctul de fierbere al benzenului
este relativ coborat (+80°C) astfel ca el se evapora usor, fapt
de care trebuie tinut seama, deoarece vaporii benzenului sunt
toxici si inflamabili. Benzenul este un solvent excelent foarte
des utilizat in industria chimica; la aceasta contribuie mult si
faptul ca fiind destul de inert chimic, nu deranjeaza mersul
reactiilor. Chiar si unii polimeri sunt solubili in benzen:
cauciucul nevulcanizat dizolvat in benzen alcatuieste cunoscuta
solutie utilizata la lipirea articolelor de cauciuc. Benzenul
este mai putin dens decat apa (densitate 0,9). Fiind in acelasi
timp nemiscibil cu apa (doua lichide care nu se solva unul in
altul) benzenul formeaza un strat deasupra apei. Aceasta insusire
este foarte pretioasa pentru practica chimiei organice, deoarece
ofera posibilitatea efectuarii operatiei de extractie cu benzen.
 |
 |
Poluarea
Poluarea
cu hidrocarburi este la ora actuala una dintre cele mai grave
probleme de mediu ale secolului in care traim si totodata o
amenintare asupra viitorului planetei noastre.
Instalatie de epurare a areului cu continut de hidrocarburi
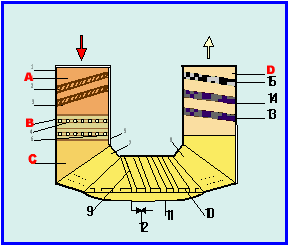 |
Domeniu
de aplicare: Epurarea aerului cu continut de hidrocarburi cu componente volatile. Descriere: Instalatia permite epurarea gazelor cu un continut complex de componente organice cu volatilitati foarte diferite. Prin constructie, filtrul realizeaza prozejarea modulului final de filtrare fina ,marind astfel ciclul de viata al instalatiei. Solutia tehnica propusa pentru epurarea aerului cu continut de hidrocarburi cu componente volatile, combina patru module de filtrare, astfel: - un modul de filtrare grosiera (A) retine componentele greu volatile; - un modul de racire (B) in care are loc condensarea vaporilor de hidrocarburi; - un modulul de colectare (C) in care a colecteaza condensul; - un modul de filtrare fina (D), unde are loc atat o filtrare fina cat si retinerea eventualilor vapori necondensati. Modulul de racire (B) este prevazut cu o baterie de racire (4) montata in interiorul unui material de umplere (6). Modulul de colectare (C) este dotat cu sicane de retinere (9) sustinute de un pod de fonta (10) si cu o cuva de recuperare pozitionata la partea inferioara (11). Modulul de filtrare fina (D) este prevazut cu casete filtrante (13), (14) confectionate din panza metalica si cu o caseta filtranta (15), ce contine un material adsorbant de tipul carbunelui activ. Avantaje: eficienta reducerii poluarii 90-95%; investitii reduse; operare usoara; dimensiuni de gabarit reduse prin combinarea celor patru module de filtrare; consum energetic redus; materiale accesibile, ieftine. |